
news
新闻中心
指南与共识 - 我国首部《非小细胞肺癌MET临床检测中国专家共识》发布.
近期,全球首部针对MET的临床检测专家共识——《非小细胞肺癌MET临床检测中国专家共识》(以下简称《共识》)正式发布,它将极大地推动MET检测的规范化,助力精准医疗的发展。

肺癌是我国最常见的恶性肿瘤之一。根据WHO发布的2020年全球最新癌症数据,我国肺癌的发病率和死亡率均高居首位。
自2003年酪氨酸激酶抑制剂吉非替尼获批以来,非小细胞肺癌(NSCLC)靶向治疗取得了突飞猛进的发展。除了常见的驱动基因外,MET等其他的少见驱动基因也受到越来越多的关注。
2021年,MET抑制剂赛沃替尼在中国正式获批,用于携带MET基因第14 号外显子跳跃突变(下文统称为MET 14跳突)的局部晚期或转移性NSCLC。MET基因扩增是EGFRTKI靶向治疗重要的耐药机制之一,多个临床试验数据表明,MET基因扩增的晚期NSCLC患者可从MET抑制剂治疗中获益,因此在中国临床肿瘤学会、非小细胞肺癌分子病理检测临床实践指南(2021 版)以及美国国家综合癌症网络(NCCN)中也被推荐检测。
《共识》主要对MET 14跳突、MET 基因扩增、 MET蛋白过表达3 种MET异常形式的临床意义、适用人群、检测方法及路径、尚存问题等进行了详尽阐述,并提出了相关建议和推荐方案;同时对检测报告的形式也进行了规范,以期指导临床进行规范的 MET检测,获得准确的检测结果,使相关患者最大化获益。
本文旨在针对MET基因扩增的相关内容进行展示
一、MET基因及临床意义
【共识2】 MET基因扩增是NSCLC的原发驱动基因变异,也是EGFRTKI和ALK-TKI耐药的重要机制之一,可作为晚期患者耐药后联合靶向治疗的潜在分子标志物,临床应重视MET基因扩增检测。
MET基因扩增是指该基因拷贝数增加,包括局部扩增和多体2种形式。MET基因扩增可作为原发性肿瘤驱动基因变异之一,多种实体肿瘤中都有发现,NSCLC中原发MET基因扩增发生比例为1%~5%。MET基因扩增与较高的组织学分级、较晚的临床分期以及不良预后相关。
有限的临床研究数据(PROFILE 1001研究,GEOMETRY mono1 研究,VISION研究)均提示MET抑制剂可能为原发MET基因扩增的晚期NSCLC患者带来获益(不同研究的原发MET基因扩增阈值有一定差异)。
MET基因扩增更常继发于其他驱动基因阳性NSCLC患者靶向治疗后,是EGFR-TKI耐药的重要机制之一。不同代EGFR-TKI耐药后出现MET基因扩增比例不尽相同,根据文献数据,第一、二代EGFR-TKI 耐药后MET基因扩增的比例为5%~22%,第三代EGFR-TKI 奥希替尼一线耐药后MET 基因扩增比例为7%~15%,二线耐药后为5%~50%。除EGFR-TKI外,MET基因扩增也是ALK-TKI 耐药机制之一,第二、三代 ALK-TKI 耐药后MET基因扩增的比例约为13%。
临床研究数据表明,EGFR-TKI 联合MET抑制剂可能是继发MET基因扩增导致的EGFR-TKI 耐药患者的潜在治疗策略。TATTON研究数据表明,EGFR-TKI耐药后MET 局部扩增和多体的患者,奥希替尼联合赛沃替尼治疗均显示出一定的临床疗效,其中MET基因扩增总体人群(n=53)的客观缓解率达到30%,局部扩增人群(n=35)和多体人群(n=18)的客观缓解率分别为31%和28%。SAVANNAH研究结果表明奥希替尼耐药后MET高扩增(FISH GCN≥10)的患者奥希替尼联合赛沃替尼治疗显示出良好的临床疗效。另有报道显示,ALK-TKI耐药后发生MET基因扩增的患者应用MET抑制剂治疗也取得了一定的疗效,值得进一步探索和研究。
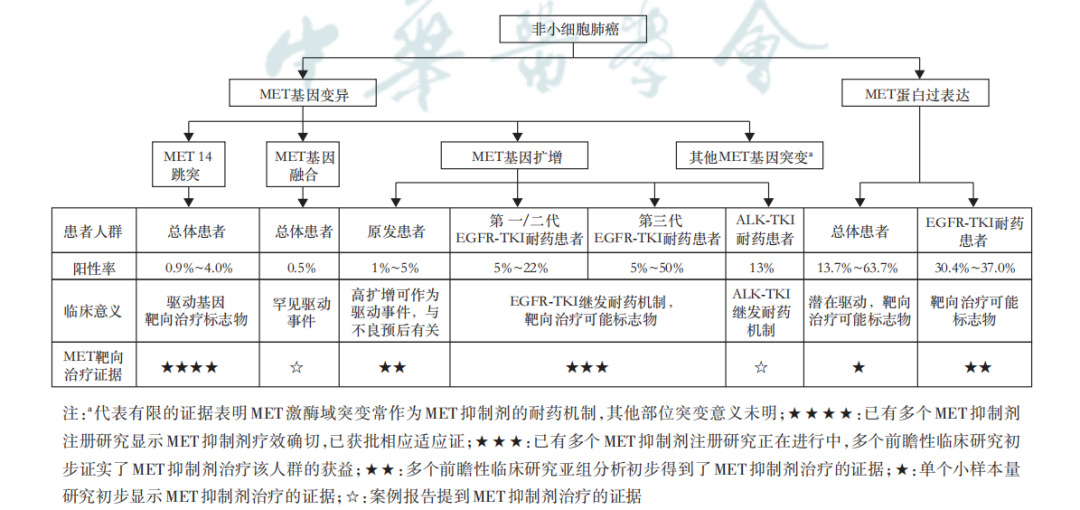
非小细胞肺癌中MET异常的发生率和临床意义
二、MET检测的适用人群
【共识4】 晚期NSCLC患者强烈推荐进行MET 14跳突检测;晚期初治和EGFR-TKI 耐药后NSCLC患者推荐进行MET基因扩增检测。
三、常见送检样本类型与处理
用于MET检测的样本类型主要包括肿瘤组织样本、细胞学样本以及液体样本等。MET 14跳突可用RNA进行检测,相关样本应注意及时固定以及样本保存条件,以防RNA降解。
1. 肿瘤组织样本:优先使用肿瘤组织石蜡样本,包括手术和活检样本,检测前需对肿瘤细胞比例评估,确保满足检测要求,对于手术样本,优先选取肿瘤细胞比例较高的样本进行检测。
2.细胞学样本:包括胸腹腔积液、支气管刷检、支气管内超声引导细针穿刺活检样本、痰、肺泡灌洗液等。需作细胞评估后进行检测,或制作成石蜡包埋样本,评估满足检测要求后进行检测。
3. 液体活检样本:对于不能获得组织或细胞学样本的晚期NSCLC患者,MET 14跳突可考虑血液检测。患者血浆中存在循环肿瘤DNA(ctDNA),可进行基因检测。部分发生脑膜转移的晚期NSCLC患者脑脊液对颅内肿瘤的ctDNA具有富集作用,也可考虑获取脑脊液进行相关检测。与组织样本相比,血液和脑脊液中ctDNA含量很低,与组织样本检测相比灵敏度较差。
四、常用MET检测方法
【共识6】 MET基因扩增可采用FISH和二代测序进行检测,FISH是检测MET基因扩增的金标准,二代测序检测MET基因扩增尚需进一步优化和验证。
MET基因扩增的检测方法目前主要包括FISH、二代测序等。目前MET基因扩增的判断标准和临床获益阈值均尚未明确,因此,本共识仅基于已发表文献数据以及临床研究中常用的检测方法和参考标准(表2)进行推荐,未来基于临床研究数据尚需进一步明确。
1. FISH:FISH技术通过荧光探针原位标记MET基因,可以结合形态直接观察肿瘤细胞中MET荧光信号的数量,来计算肿瘤细胞中MET基因GCN;或者通过标记MET基因和第7号染色体着丝粒(CEP7),计算肿瘤细胞中MET/CEP7比值。临床可以通过MET GCN以及MET/CEP7比值来判断扩增情况,该法可区分局部扩增和多体,目前是检测MET基因扩增的金标准。FISH检测MET基因扩增尚无统一的判读标准,目前主要参考UCCC标准和Cappuzzo标准。针对EGFR-TKI耐药后MET基因扩增相关的临床试验中,主要采用MET GCN≥5或MET/CEP7≥2作为入组标准,本共识推荐该入组标准作为判读参考阈值。当MET/CEP7≥2时,判断为局部扩增;当MET GCN≥5且 MET/CEP7<2时,判断为多体。后续根据临床研究的结果,具有疗效预测价值的MET基因扩增阈值可能会有调整。
 非小细胞肺癌MET基因扩增常见检测方法
非小细胞肺癌MET基因扩增常见检测方法
2. DNA二代测序:DNA二代测序方法可以基于测序深度和特定位点变异频率等信息对检测 MET基因拷贝数变异进行计算,首选肿瘤组织样本或细胞学样本。不同公司或实验室使用的二代测序检测 panel和生物信息分析策略可能有所不同,检测结果的呈现形式也可能不同。临床研究中目前多采用FISH方法入组MET基因扩增患者,已有报道组织二代测序(肿瘤细胞比例≥10%,测序深度≥500×)与FISH检测MET基因扩增的阳性一致性约为62.5%,TATTON研究中组织二代测序(肿瘤细胞比例≥20%,测序深度≥200×)与FISH检测MET基因扩增的阳性一致性为48%,进一步分析发现二代测序与FISH检测的MET局部扩增阳性一致性为88%,与 FISH 检测的MET多体阳性一致性仅为4%。二代测序检测MET基因扩增有待进一步优化和验证,因此建议临床选用经NMPA批准或经充分验证的二代测序产品对MET基因扩增进行检测。在EGFR-TKI耐药后进行检测时,由于穿刺活检获取组织样本存在挑战,血液样本也是重要的检测样本来源。TATTON研究中,与组织FISH检测相比,ctDNA二代测序检测MET基因扩增的阳性一致性为25%(局部扩增43%,多体10%)。因此,现阶段血液二代测序检测MET基因扩增仍存在挑战,需要进一步的优化验证,应优先采用组织样本进行检测。若受限于样本进行血液检测时,检测阴性不能排除MET基因扩增,必要时考虑二次活检FISH复测。
3. MET基因扩增新方法探索:微滴式数字PCR(ddPCR)是对微滴体系进行扩增反应以后,分析每个微滴的荧光信号,将判断结果按照泊松分布的原理,通过读取靶标和内参核酸的阳性微滴个数以及比例从而得到靶分子的拷贝数及浓度,在MET基因扩增检测尤其血液检测领域已有相关探索。但该方法在临床应用前尚需进一步优化和验证。
五、MET检测路径
【共识7】 晚期NSCLC MET检测首选肿瘤组织/细胞学样本,采用包括 MET的多基因联检平台(RT-qPCR或二代测序)检测MET 14跳突,DNA 二代测序检测结果阴性时,可考虑采用RNA样本补充检测;晚期NSCLC患者尤其是EGFR-TKI耐药后患者推荐FISH检测MET基因扩增。当组织/细胞学样本不可及时,可选择液体活检样本进行MET 14跳突的检测。
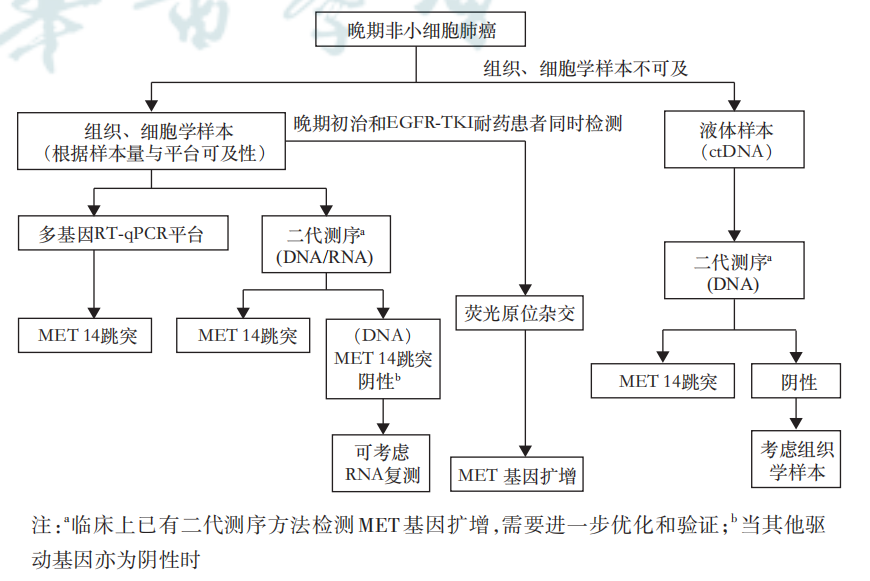 非小细胞肺癌MET检测路径
非小细胞肺癌MET检测路径
六、MET检测报告规范和其他注意事项
检测报告应包括患者基本信息、样本病理信息、检测方法、检测试剂及检测系统、质量控制信息、检测结果、变异解读、临床注释及必要的备注等核心信息。在报告的备注部分,建议包括检测方法局限性、检测中的特殊情况及进一步工作等信息。
MET基因扩增报告规范:
在FISH检测报告中建议至少包括评估的肿瘤细胞数量、平均MET拷贝数/细胞、平均CEP7拷贝数/细胞、平均MET拷贝数与平均CEP7拷贝数的比值以及发生扩增的肿瘤细胞比例等。根据判断标准确定MET基因扩增状态,阳性时应区分局部扩增和多体。
在二代测序检测报告中应包括明确的变异信息描述、基因拷贝数信息,以及检测平台本身对MET基因拷贝数变异的阳性判定阈值。对于使用液体样本进行MET基因扩增检测的二代测序报告,除上述信息外,考虑到液体检测目前灵敏度较低,报告应注明假阴性率较高等相关信息。
此外,进行MET检测的实验室应做好室内质控和室间质评,以优化规范的检测流程,确保实验操作的准确性以及检测结果的有效性。同时,由于MET异常较为复杂,临床解读MET检测结果存在一定的挑战,建议建立临床病理沟通机制,确保临床病理及时进行沟通。
虽然MET在NSCLC中属于少见驱动基因,但由于我国肺癌患者人群基数庞大,因此存在MET异常的患者为数不少。随着我国首个高选择性MET抑制剂赛沃替尼的获批上市,为MET异常的患者带来了长期生存的希望。本次《共识》的发布,将推动临床MET检测的规范化,提高MET检测的准确性,从而为MET精准治疗提供指导,惠及更多患者。

原文下载
长按二维码
点击下载